9.1.1. Schädel-Hirn-Trauma (SHT)#
Ein Schädel-Hirn-Trauma (Abkz. SHT ) ist eine Gewalteinwirkung auf den Kopf mit resultierender Funktionsstörung oder struktureller Schädigung des Gehirns.
Häufige Ursachen sind Verkehrsunfälle, Stürze und Gewalteinwirkungen. Man unterscheidet ein gedecktes SHT und ein offenes SHT. Das Leitsymptom ist die Bewusstseinsstörung.
Schweregrade (GCS)#
Die klinische Einteilung erfolgt anhand der Glasgow Coma Scale (GCS, max. 15 Punkte).
Augenöffnen (1–4)
Verbale Reaktion (1–5)
Motorische Reaktion (1–6)
Leicht: > 12
Mittel: 8–12
Schwer: ≤ 7
Die GCS erlaubt eine rasche Einschätzung der Schwere und dient der Verlaufsbeurteilung.
Formen#
Offenes SHT
Rissquetschwunden
Knochensplitter
Hirnaustritt
Liquorrhoe
Gedecktes SHT
Begleitende Verletzungen#
HWS-Verletzungen sind häufig und müssen immer mitbedacht werden.
Rissquetschwunden der Kopfhaut
Frakturen:
Schädeldach
Schädelbasis (Liquorrhoe, Monokel- oder Brillenhämatom)
Gesichtsschädel
Unterkiefer
Die Schwere des SHT lässt sich nicht zuverlässig aus äußeren Verletzungen, bzw. dem Fehlen derselben, ableiten. Eine sorgfältige Untersuchung ist obligat.
Grade#
SHT I° (Commotio, Gehirnerschütterung): Bewusstseinsstörung < 1 h
SHT II° (Contusio, Gehirnprellung): Bewusstseinsstörung > 1 h
SHT III° (Compressio, Gehirnquetschung): Bewusstlosigkeit > 24 h, schwere Schäden
Gehirnerschütterung — SHT 1°#
Die Gehirnerschütterung ist die leichteste Form des Schädelhirntraumas. Leitsymptom ist ein Trauma mit anschließender kurzer Bewusstlosigkeit. Weiters kann es zu flüchtigen neurologischen Ausfällen kommen, es kann auch eine retrograde Amnesie (Gedächtnisverlust über den Vorgang bzw. Unfall) bestehen. Eventuell klagt der Patient über Übelkeit, Erbrechen und Schwindel. Die Gehirnerschütterung zieht keine bleibenden Schäden nach sich.
Gehirnprellung — SHT 2°#
Die Gehirnprellung ist eine schwerere Form des Schädel-Hirntraumas. Leitsymptom ist die Bewusstlosigkeit länger als 1 h, beziehungsweise die Bewusstseinseintrübung < 24 h. Mittels weiterführender Diagnostik im Spital lassen sich die Hirnschädigungen nachweisen. Es kann zu Nervenverletzungen kommen, dies kann zu vegetativen Störungen führen. Bleibende Schäden sind möglich.
Gehirnquetschung — SHT 3°#
Die Gehirnquetschung ist eine sehr schwere Form des Schädelhirntraumas. Es kommt zu einer Bewusstlosigkeit länger als 24 h und zu teils sehr ausgeprägten Begleitsymptomen wie zum Beispiel Hirndruckzeichen (Hirndruckzeichen), Atem und Kreislaufstörungen bis hin zum Atemstillstand durch Einklemmen des Atemzentrums.
Es kann weiteres zu intrakraniellen Blutungen kommen (epidural, subdural, subarachnoidal). Außerdem kommt es zu verschiedenen neurologischen Ausfällen und Symptomen wie zum Beispiel zerebrale Krampfanfälle. Mit bleibenden Schäden und Langzeitfolgen ist zu rechnen.
I° |
II° |
III° |
|
|---|---|---|---|
Gehirnerschütterung |
Prellung |
Quetschung |
|
… cerebri* |
Commotio |
Contusio |
|
Bewusstlosigkeit / Trübung |
< 1h |
1 h < x < 24 h |
> 24 h |
Symptome |
Übelkeit, Erbrechen, Schwindel Evtl. flüchtige neurologische Ausfälle Retrograde Amnesie (kann sich an den Unfallhergang nicht erinnern ) Keine bleibenden Schäden |
Nachweisbare Gehirnschädigung / bleibende Ausfälle Evtl. Gehirnnervenabrisse vegetative Störungen |
Atmungs-/ Kreislaufstörungen Hirndrucksymptomatik Evtl. Einklemmung des Atemzentrums → zentraler Atemstillstand Behinderung der Hirndurchblutung Hirnblutungen, Lähmungen, zerebrale Krämpfe |
Gefahren#
Luzides Intervall: Initial symptomfreies Intervall mit späterer rascher Verschlechterung. Cave Fehleinschätzung der Schwere!
Intrakranielle Blutung
Hirndrucksteigerung: Sowohl durch eine Hirnblutung, als auch durch ein verletzungsbedingtes Anschwellen des Hirngewebes (Hirnödem) kann es zu einer Drucksteigerung innerhalb des Schädels und zum Auftreten von Hirndruckzeichen (Hirndruckzeichen) kommen.
Hirnstammeinklemmung: Da sich im Hirnstamm das Atem- und Kreislaufzentrum befindet besteht dabei akute Lebensgefahr!
Hinweise auf Einklemmung sind Mydriasis, Streckkrämpfe, vegetative Entgleisung oder Bradykardie
Herniationstypen
Transtentoriell (uncal): Kompression des N. oculomotorius → ipsilaterale Mydriasis.
Subfalzin: Verlagerung unter der Falx cerebri.
Tonsillär: Einklemmung im Foramen magnum → Atemstillstand.
Transkalvariell: Herniation durch Knochendefekte.
Atmungsstörungen u. a. aufgrund einer direkten oder indirekten Hirn- bzw. Rückenmarksschädigung
Gefahr
Das luzide Intervall kann zu einer gefährlichen Fehleinschätzung führen.
Diagnostik#
Neurostatus:
GCS
Pupillen (Hirndruckzeichen; Größe, Seitendifferenz, Lichtreaktion)
Mydriasis bei 35-40 ICP (Seitendifferenz, Herdblick bei Insult zur Ischämieseite, bei Blutung zur Gegenseite)
Motorik (gezielte vs. ungezielte Schmerzreaktion)
Halbseitenzeichen
Zeichen einer Querschnittlähmung
Vigilanz: Eine Bewusstseinsstörung kann auch andere Ursachen als den gegenständlichen Unfall haben (Blutzucker, Alkohol, Exsikkose, Schlaganfall, …).
Traumacheck: Ein Traumacheck ist natürlich verpflichtend durchzuführen.
Besonders zu beachten ist die Gefahr einer hohen Querschnittslähmung, ebenso dass Schädel, HWS und BWS eine Linie bilden.
Unfallmechanismus: Hinweise auf Hochrasanztrauma oder HWS-Beteiligung. Besonders bedenklich sind Sportverletzungen im Kopf- oder Nackenbereich, ein Trauma nach Sprung ins Wasser und Stauchungsverletzungen der HWS. Ggfs. muss eine HWS-Immobilisation durchgeführt werden
SAMPLE-Schema: Alter, Notfallereignis mit Zeitpunkt, initialer Neurostatus, Allergien, Medikamente (insb. Antikoagulation), Vorerkrankungen, letzte Mahlzeit, Ereignis.
Bildgebung:
CCT + HWS
CCT-Verlaufskontrolle: bei Vigilanzverschlechterung/Somnolenz beim wachen Patienten, beim intubierten Patienten, 6h nach dem Trauma Blutungskontrolle. Hirndruckzeichen im CCT sind das Verstreichen der basalen Zisternen und Verlust der Sulci, Midlineshift mit Abklemmung der Gefäße an der Falx cerebri mit Perfusionsstop (CT-Angio, transcranieller Doppler)
Typische CCT-Zeichen:
Verstrichene basale Zisternen
Sulcusverlust
Midline-Shift
Gefäßkompression
Ggfs. Hirndruckmessung: Ein ICP-Monitoring erfolgt mittels Codman-Sonde (misst Druck im Gehirngewebe) oder EVD (misst Druck im Ventrikel).
Begleitverletzungen ausschließen: Ev. Abdomensono, C/P (Pneu, Serienrippe, Hämatothorax), Frakturen d. Extremitäten
Neurochirurgisches Konsil: OP ? (Entlastungskraniotomie, EVD (ventrikulär, lumbal), oder konservativ?
Achtung
Jedes SHT muss im Spital abgeklärt werden (Cave: luzides Intervall).
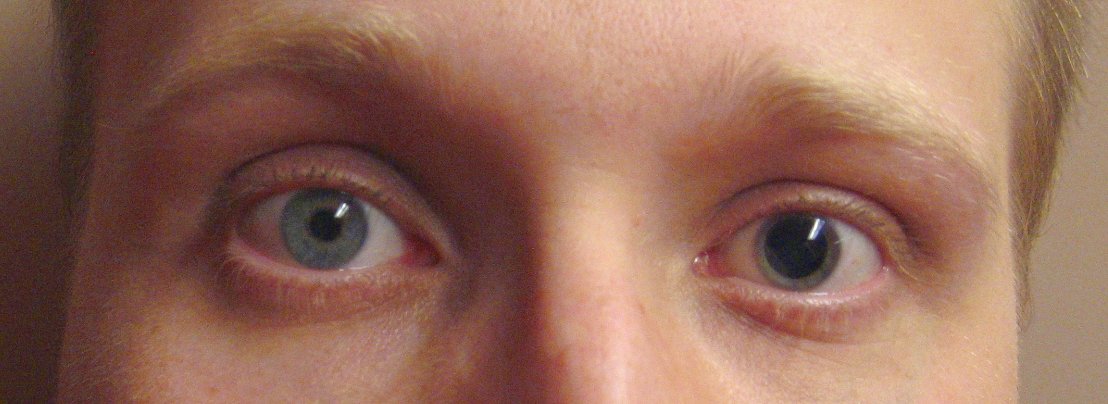
Fig. 146 Pupillendifferenz – Sie ist ein Alarmzeichen: Eine Pupillendifferenz kann ein wichtiger Hinweis auf einen erhöhten Hirndruck sein!#
© Sebastian Gabriel ℓ MfG
- Hukkelhoven Score
Alter, Motor. Reaktion, Pupillen, Hypoxie, Hypotonie, CCT, Subarachnoidales Hämatom Licox oder Raumedic-Sonde zur pO₂-Messung im Hirngewebe.
Maßnahmen#
- ⛑ Basismaßnahmen
Vitale Bedrohung beurteilen. Bei vitaler Bedrohung: Standardmaßnahmen bei vital bedrohten Patienten, Besonderheiten:
ABC-Stabilisierung
Lagerung: leicht erhöhter Oberkörper, ca. 30°, wenn keine Kontraindikation besteht.
Je nach Unfallmechanismus HWS-Immobilisation (z. B. mit Stifneck™)
Monitoring (RR, HF, SpO₂, ggf. invasiv)
≥ 2 venöse Zugänge
Oberkörperhochlagerung ca. 30°
Ggfs. HWS-Immobilisation
Wundversorgung:
Steril abdecken
Hirnmasse feucht steril abdecken
Fremdkörper nicht entfernen
Intubation bei GCS < 9:
Sicherung der Oxygenierung
Aspirationsschutz
Steuerung des ICP über paCO₂
Intensivtherapie / Neuroprotektion#
Ziel ist die Vermeidung sekundärer Hirnschädigung durch Einblutung, oder ein fokales oder diffuses Ödem: Neuroprotektion durch Vermeidung hypo- oder hypertensiver Phasen, Hirndruckkontrolle, Sicherung von Perfusion, Oxygenierung und Stoffwechsel.
ZErebraler Perfusionsdruck (CPP)
CPP = MAP − ICP
CPP: 60–70 mm Hg
Normotonie (ggf. Noradrenalin, Urapidil-Perfusor, … zur MAP-Stabilisierung)
Normovolämie (Isotone oder hypertone Lösungen; keine hypotonen Lösungen (G5 %, Ringer-Laktat)!)
Normale Serumosmolarität: Natrium 140–150 mmol / l
Normoglykämie: 120–150 mg / dl
Normothermie: < 37 °C
Hkt: > 30 %
Zielblutdruck festlegen;
Temperatur-DK,
Magensonde (Bei frontobasalen Frakturen nur oral NIE nasal!)
Intubation bei GCS < ±9 (O₂-Versorgung sichern, Aspirationsschutz, ICP-Steuerung über paCO₂, Sedierung senkt O₂-Verbrauch), RSI ev. FIO; Midazolam und Ketanest empfohlen!
ICP#
Normal: 5–15 mm Hg
Kinder: bis 2a 4-10, > 2a 20-25 (off. Fontanellen)
CPP Ng 25, Sgl. 40, Jugendlicher 70 mmHg
Klinische Korrelation:
20–40 mm Hg: Kopfschmerz, Erbrechen
35–40 mm Hg: Mydriasis
45 mm Hg: Koma, Einklemmung
Monitoring:
EVD (Goldstandard: Messung + Therapie)
parenchymale Sonde (z. B. Codman, nur Messung)
ICP-Senkung#
Oberkörperhochlagerung (15–30°)
Tiefe Analgosedierung mit Optimal Handling Kat.I (↓ CMRO₂ → ↓ CBF → ↓ ICP)
Liquordrainage EVD, neurochirurgische Entlastungsoperation
Osmotherapie:
Mannitol 0,25–1 g / kg KG: rasch verabreicht senkt den ICP bis zu 4h! Es ist hyperosmolar (1100 mosmol / l bei 20 % Lsg), führt jedoch auch zur Hypotension und Dehydrierung mit Gefahr eines prärenalem Nierenversagens und Elektrolytstörungen. Erhöht die Blutviskosität.
→ osmotischer Flüssigkeitsentzug aus dem Gehirn
Cave: Hypotonie, Nierenversagen
alternativ hypertones NaCl, Hyperhaes, TRIS (TRIS beeinflusst Liquorazidose und Ödem günstig)
Kurzfristig: Hyperventilation (paCO₂ < 30 mm Hg) bei ICP-Krise
Ev. Milde Hypothermie (33–34 °C) bei therapierefraktärem ICP
Dekompressionskraniotomie bei therapierefraktärem Druck oder raumfordernden Läsionen
- Optimal Handling Kategorisierung
Keine Körperpflege, 1 x in 12h absaugen + Tubusumlagerung + Mundpflege unter Relaxierung
Partielle Körperpflege, vertiefte Sedierung statt Relaxierung, Stuhlsorge
1xtgl. Körperpflege + Mundpflege, Physiotherapie möglich
- Chirurgische Therapie
Dekompression (osteoplastisch oder osteoklastisch) mit/ohne Hämatomentleerung, Bohrlochtrepanation. Goldstandard zur Liquordrainage ist die Ventrikelsonde, aber auch lumbal möglich.
Pathophysiologie#
Monro-Kellie-Doktrin: Intrakranielles Volumen konstant: 85 % Hirn, 5 % Liquor, 10 % Blut. Kompensation initial durch Liquorverdrängung und venöse Kompression. Danach exponentieller ICP-Anstieg.
Gehirn: ca. 20 % des O₂-Verbrauchs, ca. 15 % des Herzzeitvolumens.
CPP: CPP = MAP − ICP. Zielbereich 60–70 mm Hg.
Autoregulation: Konstanter CBF bei MAP 60–140 mm Hg, außerhalb dieses Bereiches abhängig vom MAP
paCO₂: ↑ → Vasodilatation → ICP ↑ ↓ → Vasokonstriktion → Ischämierisiko
paO₂: < 50 mm Hg → CBF ↑
Inverse-Steal-Syndrom: Umverteilung des Blutflusses von gesunden zu geschädigten Arealen. Respiratorische Alkalose kann den CBF senken und hypoxische Schäden fördern.
Cushing-Reflex: Hypertonie, Bradykardie, irreguläre Atmung (Cheyne-Stokes) bei Einklemmung
Blut-Hirn-Schranke: Tight junctions, selektiver Transport (z. B. Glukose). Störung führt zu vasogenem Hirnödem.
Hirnödem:
zytotoxisch (Zellschwellung bei Ischämie)
vasogen (BBB-Störung)
interstitiell (Liquordruck)
Liquor: Produktion ca. 150–550 ml / d, HWZ 2–6 h, mechanischer Schutz und Druckregulation.
Regulation des zerebralen Blutflusses (CBF)#
Autoregulation zwischen 60-140 MAP konstanter CBF, außerhalb dieses Bereiches abhängig vom MAP
lineare Beziehung zum paCO₂: steigt dieser um 1mmHg, steigt CBF um 2 ml / 100 g / min
paO₂-Schwellenwert: paO₂ < 50 mm Hg = steigt der CBF.
Der CPP (Cerebraler Perfusions Pressure) sollte zwischen 60 und 70mmHg liegen! (MAP – ICP = CPP)
Der intracranielle Blutfluss beträgt 14 % des Herzminutenvolumens und verbraucht 25 % des Ruhesauerstoffverbrauches.
BHS: mechanische Barriere mit Tight junctions und metabolischer Barriere, H₂O + CO₂ + O₂ kann frei diffundieren. Schützt vor Toxinen, hält Glucose im Gehirn stabil, hält Neurotransmitter im Gehirn, Kontrolliert den Elektrolyttransfer.
Liquor: Die Produktion erfolgt im Plexus choroideus, ca. 150 - 550 ml, HWZ 2-6h, Ultrafiltrat des Blutplasmas, dämpft Gehirnmasse, reguliert Atemzentrum der Medulla oblongata durch den CO₂-Gehalt.
CCT-KO: bei Vigilanzverschlechterung/Somnolenz beim wachen Patienten, beim intubierten Patienten, 6h nach dem Trauma Blutungskontrolle. Hirndruckzeichen im CCT sind das Verstreichen der basalen Zisternen und Verlust der Sulci, Midlineshift mit Abklemmung der Gefäße an der Falx cerebri mit Perfusionsstop (CT-Angio, transcranieller Doppler)
ca. 50 ml / 100 g / min
Kopplung an Stoffwechsel: ↑ CMRO₂ → ↑ CBF Sedierung → ↓ CBF
paCO₂: Änderung um 1 mm Hg → Änderung des CBF um ca. 2 ml / 100 g / min
Dynamik des ICP#
Kurzfristige ICP-Anstiege bei:
Husten
Pressen (Valsalva)
Absaugen
Umlagerung
→ Werte bis ca. 50 mm Hg möglich
Bei verminderter Compliance gefährlich.
Konsequenz: Minimal handling und ausreichende Sedierung.
Beatmung#
paCO₂ 33–36 mm Hg
paO₂ > 100 mm Hg
VT 6–8 ml / kg KG
PEEP 5–8 mm Hg (Cave: ICP-Anstieg)
I:E: E < 1,5
Pmax ca. 35 mm Hg
Bei schlechter Oxygenierung initial FiO₂ hoch, PEEP nur unter ICP-Kontrolle steigern! Cave: neurogenes Lungenödem möglich
Hyperventilation nur kurzfristig bei ICP-Krise, da Hypokapnie zu zerebraler Ischämie führen kann.
Sedierung#
Propofol bis 4 mg / kgKG (↓ zerebraler O₂-Verbrauch)
Sufentanil: analgesierend und sedierend (NW: Abhängigkeit, Darmparalyse)
Midazolam: verstärkt die Opiatwirkung
Opioide (z. B. Sufentanil)
Ketanest: beim beatmeten Patienten mit konstantem paCO₂ und stabilem MAP neuroprotektiv über NMDA-Rezeptoren (NMDA-Antagonist)
Barbiturate Thiopental oder Methohexital: senken ICP und O₂-Bedarf des Hirns, Burst-Suppression bei therapierefraktärem ICP
Ein Barbiturat-Koma bis zur Burst-Suppression im EEG wird bei therapierefraktärer Hirndruckerhöhung oder beim therapierefraktären Status epilepticus angewendet.
Clonidin: sediert und verstärkt Opiatwirkung, bei Entzugssymptomatik, Weaning (0,075-0,6 mg / h) NW: Bradykardie, selten Hypotonie (Sedierung, Sympathikolyse)
Allgemeinmaßnahmen#
Ernährung: enteraler Kostaufbau sobald möglich, initial ca. 12,5 kcal / kg KG, ab Tag 3 ca. 25 kcal / kg KG
Obstipationsprophylaxe: Erythromycin 3x 200 mg po, Gastrographin, Movichol,…
Thromboseprophylaxe: ersten 3-5 Tage bei massiver Blutung mechanische Thrombosestrümpfe, danach NMWH sc nach Rücksprache mit dem NC.
Stressulkusprophylaxe: Pantoloc, Sucralfat,…
Infektionsprophylaxe: Hygiene! Antibiotika zurückhaltend verordnen. Bei offenem SHT z.B. Cefotaxim/Claforan iv.
Dekubitusprophylaxe durch Deku-matratze
Labor / Monitoring#
S100 (Verlaufsmarker)
Kontrolle der EZ-Parameter: Leukos, CRP, PCT, IL-6
EEG: α-Wellen in Ruhe bei geschlossenen Augen, β-Wellen frontal, γ-Wellen beim Kind/Senium, δ-Wellen > 4Hz große langsame Wellen in Allgemeinnarkose. Eine Burst-Supression unter Thiopental ist eine zeitweise Unterdrückung (SUPPRESSION) der kortikalen EEG-Aktivität im Wechsel mit hochfrequenter EEG-Aktivität (BURST). Sie findet sich auch beim hypoxischen Hirnschaden.
SSEP: somatosensible evozierte Potentiale, diese werden zur Quantifizierung einer Hirnschädigung gemessen. Eine pathologische Verlängerung ist ein prognostisch schlechtes Zeichen. Bei schwerer Schädigung der Leitungsbahnen fallen sie ganz aus. (Prognose)
ggf. pO₂-Sonde (Licox)
Komplikationen#
Krampfanfälle: Therapie z. B. akut Midazolam, regelmäßig: Valproinsäure (Convulex, Depakine), Phenytoin (Epilan), Levetiracetam (Keppra), Lacosamid (Vimpat, KI bei AV-Block). Die antiepileptische Therapie kann nach dem ersten Anfall, soll nach dem zweiten und muss nach dem dritten Anfall begonnen werden.
Posttraumatischer Diabetes insipidus: durch vermind. ADH-Sekretion, ½ Amp. Minirin (= 2 µg iv. Desmopressin)
SIADH mit Wasserretention: pathologisch erhöhte Sekretion von ADH mit einer konsekutiven Retention von Wasser mit daraus folgender Verdünnungshyponatriämie
Cerebral salt wasting (Na-Verlust): Hyponatriämie mit Volumenmangel + hohes Harnnatrium
Neurogenes Lungenödem
Risikofaktoren für sekundäre Hirnschädigung#
Hypotonie
Hypoxie
Globale Ischämie bei CCP < 50 mm Hg
Regionale Ischämie bei Vasospasmus (erhöhte Flussgeschwindigkeiten im transcraniellen Doppler)
Anämie HK < 30 %
Hyperkapnie > 38 mm Hg (ICP Anstieg durch Vasodil.) und Hypokapnie < 25 mm Hg (Ischämie durch Vasokonstr.)