Chronische Bronchitis und COPD#
Die chronische Bronchitis ist eine chronische entzündliche Schleimhautschädigung der unteren Atemwege.
Die COPD (engl. Chronic Obstructive Pulmonary Disease, chronisch-obstruktive Lungenerkrankung) ist eine chronische entzündliche Schleimhautschädigung, welche eine zunehmende obstruktive Atemwegseinschränkung aufweist.
Die COPD ist durch eine voranschreitende Verschlechterung der Atemleistung gekennzeichnet. Am Anfang steht die chronische Bronchitis, welche durch Husten mit schleimigem Auswurf gekennzeichnet ist (“Raucherhusten”). Es kommt dabei zu einer gesteigerten Entzündungsantwort auf eingeatmete Stoffe (Zigarettenrauch, Umweltschadstoffe, …). Wenn man in der Lungenfunktionsuntersuchung eine Atmungsseinschränkung nachweisen kann, spricht man von der chronisch-obstruktiven Lungenerkrankung (COPD). Diese geht mit bleibenden Veränderungen der unteren Atemwege einher und sind in der Grafik Veränderung der Atemwege bei der COPD dargestellt.
Durch die erschwerte Ausatmung kommt es zu einer chronischen Überblähung der Lungenbläschen und zu einer “Fass-förmigen” Verformung des Brustkorbes. Im Endstadium zeigen sich Zeichen einer Rechtsherzinsuffizienz aufgrund einer Störung im Lungenkreislauf.
Entwicklung einer COPD-Erkrankung#
Eine COPD entsteht nicht plötzlich: Ein COPDler hat eine “Karriere” hinter sich.
© Lena Hirtler, ℓ MfG
Exazerbation#
Kommt zu der ohnehin schweren Grunderkrankung noch ein erschwerender Faktor hinzu, z. B. eine Infektion der Atemwege, kann es zu einer plötzlichen Verschlechterung kommen, zur Exazerbation. Diese ist meist durch vermehrte Atemnot, Husten und Auswurf gekennzeichnet.
Im Detail#
Chronische Bronchitis + Lungenemphysem + smal airway disease mit erhöhter Resistance durch Bronchospasmus, Schleimhaut-Hypertrophie und SH-Ödem, sowie Dyskrinie.
Charakteristisch ist der endexspiratorischer Kollaps der Bronchien (ab 16. Generation keine Knorpelspangen mehr) mit verlängertem Exspirium und endexspiratorischen Restflow (intrinsic PEEP) und Überblähung durch Airtrapping. Es kommt zu einer erhöhten FRC mit erhöhter Totraumventilation und Kapillarkompression mit erhöhtem PVR. Die Folge ist ein erhöhte isometrische Atemarbeit, da der Restflow überwunden werden muss, bevor der inspiratorische Fluss zustande kommt. Bis zu 50 % der Atemarbeit bei COPD IV ist eine somit eine flussunwirksame Atemarbeit!
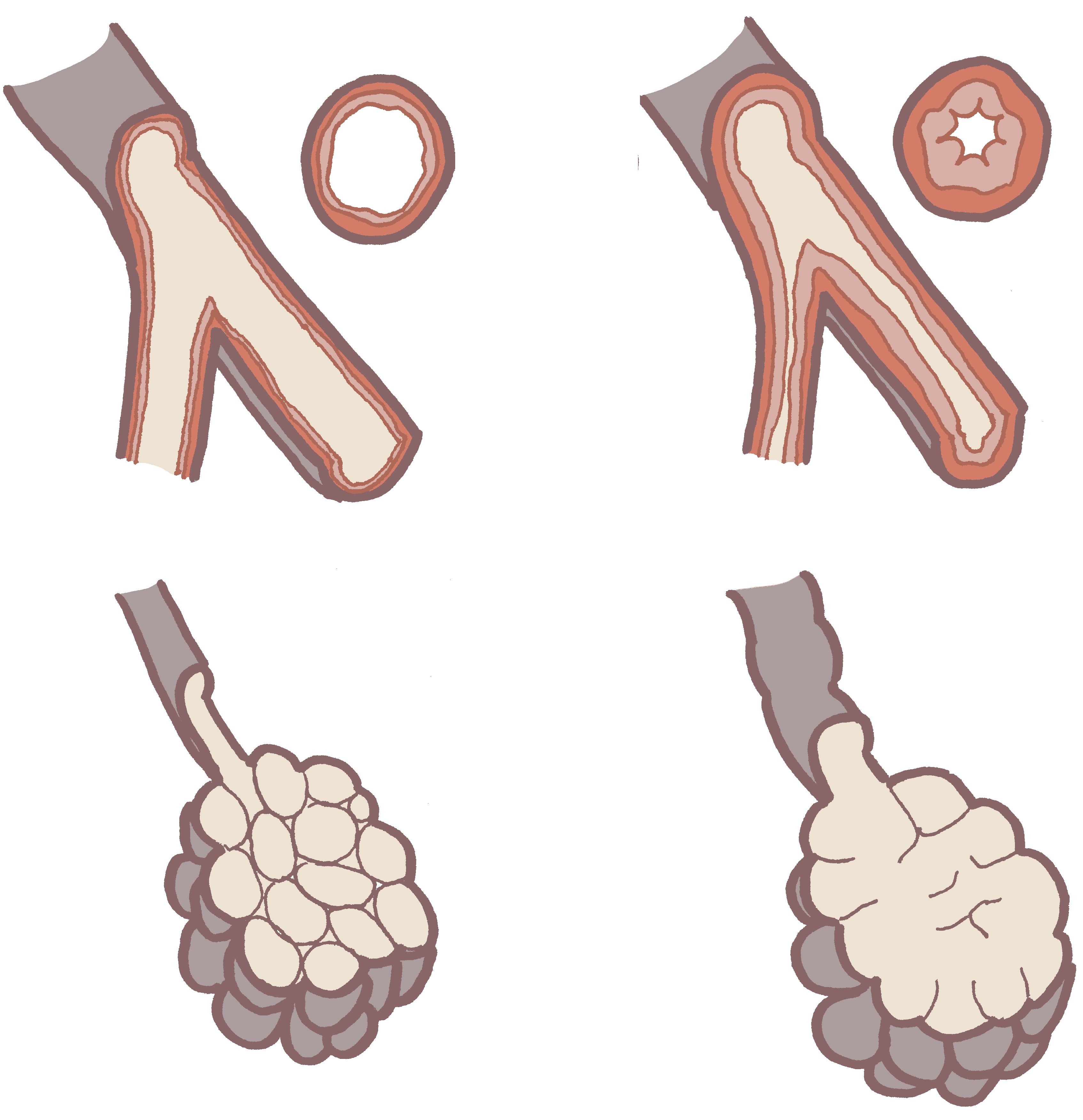
Veränderung der Atemwege bei der COPD#
Links: Schema eines gesunden Bronchus und einer gesunden Alveole. Oben rechts: Bei der COPD sind die kleinen Luftwege verschleimt und verengt. Unten rechts: Die Lungenbläschen (Alveolen) sind überbläht, weil die Luft nur erschwert wieder entweichen kann.
© Lena Hirtler ℓ MfG
Stadium |
Beschreibung |
|---|---|
I |
FEV1 > 80 %, mit/ohne Husten/Auswurf |
II |
FEV1 < 80 % mit Husten/Auswurf |
III |
FEV1 < 50 mit Husten/Auswurf |
IV |
FEV1< 30 % oder < 50 % mit chron respiratorischer Insuffizienz |
🔎 Diagnostik#
- Klinisch
Faßthorax, Pink Puffer oder Blue Bloater, hypersonorer Klopfschall bei Emphysem
- 🧪 Labor
Polyglobulie
- C/P
Emphysem mit flachen Zwerchfellkuppen
- LUFU
vermind. VK und red. FEV1, obstruktive Ventilationsstörung, Erhöhte Compliance bei verminderter Struktur (elastische Fasern zerstört), aber auch verminderte Rückstellkraft und Obstruktion = erhöhte Resistance.
- BGA
paCO₂ erhöht mit kompensiertem pH, chronische Hyperkapnie
Probleme mit Sauerstoff bei COPD-Patienten#
Beim gesunden Menschen ist der Atemantrieb vom CO₂-Gehalt des Blutes abhängig: Je höher der CO₂-Gehalt, desto stärker der Atemantrieb. Bei COPD-Patienten ist die CO₂-Konzentration im Blut jedoch chronisch erhöht, dadurch gewöhnt sich der Körper an diesen Zustand. Er beginnt dann den Atemantrieb direkt über den O₂-Gehalt im Blut zu regeln.
Dies kann bei der Behandlung Probleme bereiten: Wird bei solch einem Patienten der O₂-Gehalt künstlich erhöht (z. B. durch Sauerstoffberieselung), fehlt der Atemantrieb, es gilt bei diesen Patienten: Je höher der O₂-Gehalt des Blutes, desto geringer der Atemantrieb. Somit wird CO₂ nicht mehr ausreichend abgeatmet, der CO₂-Gehalt im Blut steigt weiter an und es kommt dadurch zu Bewusstseinsstörungen (CO₂-Narkose). Im Extremfall kann es auch zu einem Atemstillstand kommen.
Gefahr
Bewusstseinsstörungen bei übermäßiger Sauerstoffgabe möglich!
Bei COPD-Patienten kann es bei Sauerstoffgabe zu Bewusstseinsstörungen und im Extremfall zu einem Atemstillstand kommen.
Symptome der Exazerbation#
Das Leitsymtopm ist die Atemnot, häufig mit einem Angstgefühl. Je nach Schweregrad kommt es zu Zeichen einer Atemwegsverlegung der unteren Atemwege (Obstruktion, durch Verengung der Bronchien und Schleimproduktion) und Ateminsuffizienz: Die Exspiration ist erschwert, der Patient klagt über Belastungsdyspnoe, ein Engegefühl, Husten und hat Tachypnoe und evtl. eine zentrale 🚩 Zyanose. Das Exspirium ist verlängert, oft kann man ein brummendes, pfeifendes oder giemendes oder vermindertes Atemgeräusch hören.
Typisch ist der Einsatz der Atemhilfsmuskulatur (Abstützen der Arme), Mühe beim Atmen
Schon beim stabilen Patienten zeigt sich in der BGA eine Hyperkapnie (wobei der pH-Wert im chronischen Setting häufig normal ist) und Hypoxie, sowie eine verminderte Sauerstoffsättigung (~ 90 %). Bei fortgeschrittener Ateminsuffizienz bekommt der Patient oft eine Heimsauerstofftherapie verordnet. Bei akuter respiratorischer Insuffizienz kann es durch eine Hyperkapnie zu 🚩 Bewusstseinsstörungen kommen (CO₂-Narkose)! In Folge einer Rechtsherzbelastung kann es zu einem Jugularvenenstau und peripheren Ödemen kommen.
Als Nebenbefund können Infektzeichen vorliegen (erhöhte Körpertemperatur).
Bei 🚩 schwerer Atemnot oder 🚩 Bewusstseinsstörungen vitale Bedrohung.
① |
Evtl. kalte Umgebung (kalte Luft führt zur Verengung der Bronchien) |
|---|---|
② |
|
③ |
Bei schweren Anfällen kann es aufgrund der Hypoxie zu 🚩Bewusstseinsstörungen kommen. |
④ |
Atemnot, Angst, Erstickungsgefühl |
Ⓐ |
Siehe Ⓑ |
Ⓑ |
Exspiration ist erschwert, der Patient klagt über Belastungsdyspnoe, ein Engegefühl, Husten und hat Tachypnoe und evtl. eine zentrale 🚩 Zyanose. Exspirium ist verlängert, oft kann man ein brummendes, pfeifendes oder giemendes oder vermindertes Atemgeräusch hören. |
Ⓒ |
Evtl. tachkard und hyperton In Folge einer Rechtsherzbelastung kann es zu einem Jugularvenenstau und peripheren Ödemen |
Ⓓ |
|
Ⓔ |
|
… |
Als Nebenbefund können Infektzeichen vorliegen (erhöhte Körpertemperatur). |
= |
Bei 🚩 schwerer Atemnot oder 🚩 Bewusstseinsstörungen vitale Bedrohung. |
🅂 |
|
🄰 |
|
🄼 |
Inhalatoren bzw. Sprays zur Dauer- und Akuttherapie, Heimsauerstoff. Häufig Kortisonpräparate; bei vorbekanntem Infekt wurden oft schon Antibiotika verschrieben. |
🄿 |
Eine COPD ist normalerweise vorbekannt. |
🄻 |
Letzte Spray-Einnahme? |
🄴 |
|
🅁 |
℞ Therapie#
- Taktik
Linderung der Atemnot und rasche medikamentöse Therapie
Ggfs. Beatmungstherapie.
Vitale Bedrohung bei anhaltender schwerer Atemnot!
⛑ Basismaßnahmen#
Lagerung: Oberkörper hoch
Voratmen, Lippenbremse
Bei vitaler Bedrohung: Standardmaßnahmen bei vital bedrohten Patienten
O₂-Gabe: Soviel wie notwendig, so wenig wie möglich: Gefahr der CO₂-Narkose durch Hemmung des Atemantriebes!
Sauerstoff vorsichtig dosieren, anfänglich nur 2-3 L / min, weiter je nach SpO₂ oder BGA, dabei keinesfalls die Normalwerte eines Gesunden anstreben!
Wenn der Patient bereits Heimsauerstoff benutzt, 1-2 L / min höher dosieren. Heimsauerstoff soll jedenfalls weiter gegeben werden!
Atmung und Bewusstsein müssen bei der O₂-Gabe besonders sorgfältig überwacht werden!
🕏 Pharmakotherapie#
Beta-Mimetikum inhalativ: Im Allgemeinen gut verträglich, eine ausreichende Ventilation ist aber Voraussetzung!
Salbutamol (Combivent™)
Berodual™ (Fenoterol kombiniert mit Ipratropiumbromid)
Anxiolyse und leichte Sedierung mit Morphin (Vendal™)
1 Amp. Vendal™ auf 10 mL verdünnen (1 mg / mL); Start mit 2 mg, mg-weise titrieren. Cave Atemdepression!
Kortikoid i. v.: eher mittelfristige Therapie
z. B. Prednisolon 25—100 mg i. v.
Kortikoid inhalativ: eher mittelfristige Therapie
Beta-Mimetikum i. v.: wenn therapierefraktär
Terbutalin (Bricanyl™) 0,500 mg (1. Amp.) auf 10 mL verdünnen, mL-weise (0,050 mg) i. v., nach Klinik und Herzfrequenz titrieren
Alternativ s. c.-Gabe möglich: 0,250—0,500 mg s. c.
Gefahr
Cave: Tachykardie!
Theophyllin: Aufgrund der geringen therapeutischen Breite und aufgrund des großen Spektrums an Nebenwirkungen bzw. Interaktionen eher nicht empfehlenswert; bei Theophyllin-Dauertherapie Spiegelbestimmung.
Beatmungstherapie#
NIV (CPAP. CPAP+ASB), Intubation.
- Indikation zur NIV
klinische Bild: progredient zunehmende Dyspnoe, AF > 35/min, inkostale Einziehungen, Schaukelatmung, muskuläre Erschöpfung.
paCO₂> 55 steigende Tendenz, paO₂ < 55 mit SaO₂< 88 trotz Sauerstoffgabe, pH < 7,3
- Voraussetzung für NIV
Kooperativer Patient, evtl. leichte Sedierung mit Morphin erwägen.
- Beatmungseinstellung NIV
CPAP oder CPAP-ASB.
PEEP schrittweise steigern, Druckunterstützung 5-10 CPAP-ASB. PEEP ist nicht zum öffnen der Alveolen, diese sind emphysematös überbläht, sondern zur Reduktion der Atemarbeit!
PEEPe < PEEPi!
Der extrinsische PEEP muss UNTER dem intrinsischem PEEP liegen = Reduktion der Atemarbeit (innere Schienung) + Offenhalten der kleinen Atemwege (vermindert Resistance).
Bei CPAP-ASB Rampe max 0,2sec (darüber Verlängert sich die Inspirationszeit auf Kosten der Exspirationszeit mit Erhöhung des intrinsischem PEEP und der isometrischen Atemarbeit)
Warnung
Cave: Desynchronisation zwischen Patient und Respirator: Bei zu hohem intrinsischem PEEP reicht die Eigenanstrengung des Patienten nicht aus um eine Druckunterstützung zu triggern. Folglich ist die Atemfrequenz des Patienten größer als die des Respirators. Ursache kann ein enger Tubus, sehr hohe AF, hohe Triggerschwelle, flache Rampe, hoher ASB-Druck mit zu hohem AMV sein.
Therapie: Ursache beheben, exspiratorischen PEEP anheben.
- Kriterien zur Intubation
Zunehmende Somnolenz,
unzureichende Schutzreflexe,
rapid shallow breathing (AF> 35/min, VT < 300),
weiterer paCO₂ Anstieg mit pH-Abfall,
zunehmende hämodynamische Instabilität,
Schocksymptomatik,
HF > 140/min.
Tipp
Intubation so restriktiv wie möglich – als Ultima ratio falls trotz Therapie respiratorische Insuffizienz bestehen bleibt.
Die Entwöhnung kann extrem schwierig sein!
Palliative Therapie#
Die COPD ist eine chronische, oft mit viel Leid verbundene, Erkrankung. Es ist möglich, dass der Patient bereits im Vorfeld Therapieentscheidungen getroffen hat, bzw. das Stadium oder der Fortschritt der Erkrankung die Indikation zur palliativen Therapiestrategie stellt. Einzelfallentscheidung!
Perioperatives Management#
Anamnese: Verändeurng der Leistungsfähigkeit?
Lungenfunktion und pulmologische Vorstellung wenn Belastungsdyspnoe oder Veränderung der Leistungsfähigkeit
Wenn möglich, Regionalanästhesie
Bei Allgemeinnarkose
Inhalationsanästhetika (VIA) mit broncholytischer Wirkung bervorzugen
Tagesklinischen Vorgehen nicht möglich
Die inhalative bzw. bronchospasmolytische Therapie wird bis zuletzt fortgesetzt!
Sprays bzw. Dosieraerosole sollen in den OP mitgenommen werden